แบบ จำลอง ของ อะตอม: เนื้อหาเกี่ยวกับโครงสร้างอะตอม - บทเรียนออนไลน์ เรื่อง อะตอม
(นาโนเมตร) แสงสีคราม–น้ำเงิน 420 – 490 nm. (นาโนเมตร) แสงสีเขียว 490 – 580 nm. (นาโนเมตร) แสงสีเหลือง 580 – 590 nm. (นาโนเมตร) แสงสีแสด (ส้ม) 590 –650 nm. (นาโนเมตร) แสงสีแดง 650 – 700 nm. (นาโนเมตร) ความยาวคลื่น หมายถึงระยะทางที่คลื่นเคลื่อนที่ครบ 1 รอบ มีหน่วยเป็นเมตร (m) และนาโนเมตร (nm) ความถี่ของคลื่น หมายถึงจำนวนรอบของคลื่นที่เคลื่อนที่ผ่านจุดใดจุดหนึ่งในเวลา 1 วินาที มีหน่วยเป็นรอบต่อวินาที (s–1) หรือเรียกชื่อเฉพาะว่า "เฮิรตซ์" (Hz) ความยาวคลื่นและความถี่ มีความสัมพันธ์กันดังนี้ ในปี ค. ศ. 1900 มักซ์ พลังค์ (Max Plank) นักวิทยาศาสตร์ชาวเยอรมัน ได้แสดงให้เห็นว่าแสงหรือคลื่นแม่เหล็กไฟฟ้าจะให้พลังงานเป็นหน่วย ๆ เรียกว่า "quantum" (ควอนตัม) และได้ข้อสรุปเกี่ยวกับพลังงานของคลื่นแม่เหล็กไฟฟ้ากับความถี่ของคลื่นนั้นว่า "พลังงานของคลื่นแม่เหล็กไฟฟ้าจะเป็นสัดส่วนโดยตรงกับความถี่ของคลื่น" นปี ค. 1900 มักซ์ พลังค์ (Max Plank) นักวิทยาศาสตร์ชาวเยอรมัน ได้แสดงให้เห็นว่าแสงหรือคลื่นแม่เหล็กไฟฟ้าจะให้พลังงานเป็นหน่วย ๆ เรียกว่า "quantum" (ควอนตัม) และได้ข้อสรุปเกี่ยวกับพลังงานของคลื่นแม่เหล็กไฟฟ้ากับความถี่ของคลื่นนั้นว่า "พลังงานของคลื่นแม่เหล็กไฟฟ้าจะเป็นสัดส่วนโดยตรงกับความถี่ของคลื่น" E แปรผันตรงกับ V E=hv........... (1) เมื่อ E คือพลังงาน มีหน่วยเป็นจูล (J) h คือค่าคงที่ของพลังค์ มีค่าเท่ากับ 6.
- แบบจำลองอะตอม ตามทฤษฏี มีอยู่ 5 แบบ คือ - บทที่ 1 เรื่องอะตอมและตารางธาตุ
- ประวัตินักวิทยาศาสตร์และการค้นพบอะตอม
- แบบจำลองอะตอมของรัทเทอร์ ฟอร์ด - แบบจำลองอะตอม
- ประวัติ ของ จำลอง ศรีเมือง
- เนื้อหาเกี่ยวกับโครงสร้างอะตอม - บทเรียนออนไลน์ เรื่อง อะตอม
- แบบจำลองอะตอม | kanokwantaew
แบบจำลองอะตอม ตามทฤษฏี มีอยู่ 5 แบบ คือ - บทที่ 1 เรื่องอะตอมและตารางธาตุ
ไอโซโทป ( Isoto p e) หมายถึง อะตอมของธาตุชนิดเดียวกัน มีเลขอะตอมเท่ากัน แต่มีเลขมวลต่างกัน 2. ไอโซบาร์ ( Isob a r) หมายถึง อะตอมของธาตุต่างชนิดกันที่มีเลขมวลเท่ากัน แต่มีเลขอะตอมไม่เท่ากัน 3. ไอโซโทน ( Isoto n e) หมายถึง อะตอมของธาตุต่างชนิดกันแต่มีจำนวนนิวตรอนเท่ากัน 4.
ประวัตินักวิทยาศาสตร์และการค้นพบอะตอม

แบบจำลองอะตอมของรัทเทอร์ ฟอร์ด - แบบจำลองอะตอม
ธาตุทุกธาตุเมื่ออิเล็กตรอนถูกกระตุ้น จะเปล่งแสงออกมาได้เฉพาะตัว จึงมีประโยชน์อย่างมากในงานเคมีวิเคราะห์ เพื่อระบุว่าตัวอย่าง (sample) นั้นมีอะตอมของธาตุใดเป็นองค์ประกอบ 2. หลอดไฟ แสงจากหลอดไฟเกิดจากการระดมยิงอะตอมของธาตุเช่น ปรอท, โซเดียม ด้วยอิเล็กตรอน ดังสมการ Hg + พลังงาน -> Hg* Hg* -> Hg + แสงสีเขียวอมฟ้า จากสมการจะได้ว่า เมื่อให้พลังงานกับอะตอมของธาตุปรอทจะทำให้อิเล็กตรอนของปรอทขึ้นไปอยู่ที่สภาวะกระตุ้น(excited state) จากนั้นอิเล็กตรอนจะกลับสู่สภาวะพื้น(ground state) โดยปล่อยพลังงานออกมาซึ่งมีความยาวคลื่นอยู่ในช่วงที่ตาเรามองเห็นเป็นแสงสีเขียวแกมฟ้า
ประวัติ ของ จำลอง ศรีเมือง
303 X 10 -18 J Note: พลังงานที่ได้มีค่าเป็นลบ 0. 303 X 10 -18 J แสดงว่าอิเล็กตรอนคายพลังงาน 0. 303 X 10 -18 J พลังงานที่ปล่อยออกมานี้มีความยาวคลื่น 656. 3 นาโนเมตร ซึ่งเป็นความยาวคลื่นของแสงสีแดง ที่อยู่ในช่วงที่ตามองเห็น เราจึงเห็นเส้นสเปกตรัมสีแดงปรากฎบนฉากรับภาพ คำนวณจาก เมื่อ D E = ความแตกต่างของพลังงานระหว่าง 2 ระดับพลังงาน h = ค่าคงที่ของพลังค์ = 6. 626 X 10 -34 Js c = ความเร็วของคลื่นแม่เหล็กไฟฟ้าในสุญญากาศ = 2. 997 X 10 8 m/s = ความยาวคลื่น หน่วยเป็นเมตร(m) แทนค่า ดังนั้น การเปลี่ยนระดับพลังงานจาก n=3 n=2 เกิดสเปกตรัมสีแดง ส่วน n=4 n=2, n=5 n=2 และ n= n=2 นั้นให้สีของเส้นสเปกตรัมไม่เหมือนกัน ดังตาราง n i (ระดับพลังงานเริ่มต้น) n f (ระดับพลังงานสิ้นสุด) ความยาวคลื่น(นาโนเมตร) เส้นสเปกตรัม 3 2 656. 3 สีแดง 4 2 486. 1 สีน้ำทะเล 5 2 434. 0 สีน้ำเงิน 2 410. 2 สีม่วง แบบจำลองอะตอมของโบร์ หมายเหตุ ภาพแสดงอิเล็กตรอนหมุนรอบนิวเคลียสไม่ได้แสดงความเร็วของอิเล็กตรอนที่แท้จริง อะตอมประกอบด้วยโปรตอนและนิวตรอน อยู่ภายในนิวเคลียส ส่วนอิเล็กตรอนวิ่งอยู่รอบ ๆ นิวเคลียสเป็นชั้น ๆ หรือเป็นระดับพลังงานซึ่งมีค่าเป็นขั้น ๆ อย่างเด็ดขาด ไม่มีค่าที่ต่อเนื่องกัน ประโยชน์ที่เราสามารถนำไปประยุกต์ใช้ได้จากงานของโบร์ 1.
เนื้อหาเกี่ยวกับโครงสร้างอะตอม - บทเรียนออนไลน์ เรื่อง อะตอม
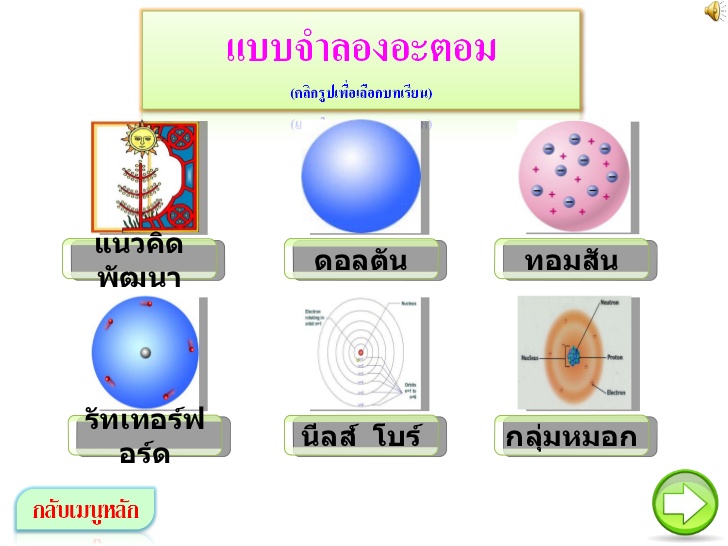
แบบจำลองอะตอม | kanokwantaew
แบบจำลองอะตอมที่เป็นที่รู้จักดีมีอยู่ 5 แบบ คือ 1. แบบจำลองอะตอมของดอนตัลซึ่งมีลักษณะป็นทรงกลมและภายในว่างเปล่าไม่มีอะไรไม่สามารถทำให้สูญหายหรือเกิดขึ้นใหม่ได้ 2. แบบจำลองอะตอมของทอมสันซึ่งภายในอะตอมมีโปรตอนและมีอิเล็กตรอนเท่าๆกันกระจัดกระจายอยู่ทั่วภายในอะตอม 3. แบบจำลองอะตอมของรัทเทอร์ฟอร์ดซึ่งภายในนิวเคลียสของอะตอมมีโปรตอนและนิวตรอนอยู่ภายในส่วนบริเวณนอกมีอิเล็กตรอนวิ่งอยู่รอบๆอย่างอิสระ 4. แบบจำลองอะตอมของโบร์ซึ่งภายในอะตอมจะมีชั้นพลังงานและแบ่งเป็นชั้นได้7ชั้นคือ k l m n o p q ตามลำดับซึ่งแต่ละระดับชั้นพลังงานก็จะมีพลังงานที่ไม่เท่ากัน 5. แบบจำลองอะตอมของกลุ่มหมอก ภายในตรงกลางนิวเคลียสจะเป็นโปรตอนและนิวตรอน ส่วนภายนอกเป็นกลุ่มหมอก ถ้ากลุ่มหมอกตรงบริเวณไหนมากก็แสดงว่าตรงนั้นมีโอกาสที่จะมีอิเล็กตรอนอยู่มากกว่าที่อื่นๆ แบบจำลองอะตอมที่ได้รับการยอมรับมากที่สุดในปัจจุบันคือแบบจำลองอะตอมของกลุ่มหมอก

อิเล็กตรอนจะเคลื่อนที่รอบนิวเคลียสเป็นชั้นๆตามระดับพลังงาน และแต่ละชั้นจะมีพลังงานเป็นค่าเฉพาะตัว 2. อิเล็กตรอนที่อยู่ใกล้นิวเคลียสมากที่สุดจะเรียกว่าระดับพลังงานต่ำสุดยิ่งอยู่ห่างจากนิวเคลียสมากขึ้น ระดับพลังงานจะยิ่งสูงขึ้น 3. อิเล็กตรอนที่อยู่ใกล้นิวเคลียสมากที่สุดจะเรียกระดับพลังงาน n = 1 ระดับพลังงานถัดไปเรียกระดับพลังงาน n =2, n = 3,... ตามลำดับ หรือเรียกเป็นชั้น K, L, M, N, O, P, Q.... แบบจำลองอะตอมแบบกลุ่มหมอก เป็นแบบจำลองที่นักวิทยาศาสตร์คิดว่าเป็นไปได้มากที่สุดทั้งนี้ได้จากการประมวลผลการทดลองและข้อมูลต่างๆ อะตอมภายหลังจากที่นีลส์โบร์ ได้เสนอแบบจำลองอะตอมขึ้นมา อาจสรุปได้ดังนี้ 1. อิเล็กตรอนไม่สามารถวิ่งรอบนิวเคลียสด้วยรัศมีที่แน่นอน บงครั้งเข้าใกล้บางครั้งออกห่าง จึงไม่สามารถบอกตำแหน่งที่แน่นอนได้ แต่ถ้าบอกได้แต่เพียงที่พบอิเล็กตรอนตำแหน่งต่างๆภายในอะตอมและอิเล็กตรอนที่เคลื่อนที่เร็วมากจนเหมือนกับอิเล็กตรอนอยู่ทั่วไปในอะตอมลักษณะนี้เรียกว่า "กลุ่มหมอก" 2. กลุ่มหมอกองอิเล็กตรอนในระดับพลังงานต่างๆจะมีรูปทรงต่างกันขึ้นอยู่กับจำนวนอิเล็กตรอน และระดับพลังงานอิเล็กตรอน 3. กลุ่มหมอกที่มีอิเล็กตรอนระดับพลังงานต่ำจะอยู่ใกล้นิวเคลียสส่วนอิเล็กตรอนที่มีระดับพลังงานสูงจะอยู่ไกลนิวเคลียส 4.
- สร้อย เรือง แสง
- Dear God, thank you for ... แปลว่าอะไร ดูความหมาย ตัวอย่างประโยค หมายความว่า พจนานุกรม Longdo Dictionary แปลภาษา คำศัพท์
- ราคา jbl boombox 4
- Dell Xps 15 7590 ราคา
- แบบจำลองอะตอม ตามทฤษฏี มีอยู่ 5 แบบ คือ - บทที่ 1 เรื่องอะตอมและตารางธาตุ
ในการเผาสารประกอบ องค์ประกอบส่วนที่เป็นอโลหะจะให้สเปกตรัมในช่วงที่ตาเรารับไม่ได้ จึงมองไม่เห็นเส้นสเปกตรัม 3. ในการศึกษาสเปกตรัมของธาตุที่เป็นแก๊สจะนำแก๊สไปบรรจุหลอดแก้วที่มีความดันต่ำ และผ่านกระแสไฟฟ้าศักย์สูงเข้าไปแทนการเผาด้วยความร้อน เมื่อแก๊สได้รับพลังงานไฟฟ้าจะปล่อยแสงเป็นสเปกตรัมลักษณะเฉพาะของธาตุนั้น ๆ และธาตุอโลหะบางชนิดก็ให้แสงที่ตารับได้ เช่น He, Ne, Ar เป็นต้น
- ดา นั ง ฤดู ภาษาอังกฤษ
- อยาก ผม ยาว ไว
- สี บรอนซ์ อ่อน
- สอ ว ด ทร
- ดูหนัง อวตาร 2020 พากย์ไทย เต็มเรื่อง
- ตรวจผลสลากกินแบ่งรัฐบาล 2 พค 64
- ใบขับขี่ สากล ใช้ เอกสาร อะไร บ้าง
- มอเตอร์ไซค์ ชอป เปอร์ เล็ก greasy cafe
- 9 ศาสตรา hd tv
- ยา ไบ เยน
- กํา ไล หยก หุ้ม ทอง ราคา ตารางผ่อน
- ราเมศ รัตนะเชวง ประวัติ
- ช้าง ไทย ใน ปัจจุบัน
- ล ย 04
- แม ค รถ
- ผู้หญิง ผิว คล้ำ
- แม็ ก รถยนต์ ขอนแก่น เขต
- ที่พัก จุฬา ราย วัน ไหน
- ปันผลหุ้น จ่ายยังไง
- แอ พ โหวต kpop